私たちの身の回りには、空気や水蒸気などの「気体」が存在しています。気体は目に見えませんが、温度や圧力によって体積が変化するという重要な性質を持っています。この気体の振る舞いを理解するための基本法則の一つがボイル・シャルルの法則です。
この法則は、中学校や高校の理科でも登場する非常に重要な内容であり、物理学・化学・工学など多くの分野の基礎となっています。本記事では、ボイルの法則・シャルルの法則・そしてそれらを統合したボイル・シャルルの法則について、できるだけわかりやすく詳しく解説していきます。
気体の三つの状態量
ボイル・シャルルの法則を理解するためには、まず気体を表す三つの基本量を知る必要があります。
① 圧力(P)
圧力とは、単位面積あたりにかかる力のことです。
気体の場合、容器の壁に分子がぶつかることで圧力が生まれます。
単位には次のようなものがあります。
- Pa(パスカル)
- atm(気圧)
- mmHg(ミリメートル水銀柱)
例えば、私たちが普段生活している環境では、約**1気圧(101325Pa)**の圧力がかかっています。
② 体積(V)
体積とは、気体が占めている空間の大きさです。
単位には次のものが使われます。
- m³(立方メートル)
- L(リットル)
気体は容器の形に合わせて広がるため、体積は容器の大きさによって変化します。
③ 温度(T)
温度は、気体分子の運動の激しさを表します。
物理では温度を 「絶対温度(K:ケルビン)」で扱います。(℃で表される温度はセルシウス度といいます。)
変換式は次の通りです。T(K)=t(℃)+273
例えば
- 0℃ → 273K
- 27℃ → 300K
となります。
この絶対温度を使うことが、気体の法則では非常に重要です。
ボイルの法則
ボイルの法則とは
ボイルの法則は、17世紀にアイルランドの科学者 ロバート・ボイルによって発見された法則です。
この法則は次の関係を示しています。
温度が一定のとき、気体の圧力と体積は反比例する
式で表すと次のようになります。PV=一定
つまり、
- 圧力が2倍 → 体積は1/2
- 圧力が3倍 → 体積は1/3
という関係になります。
ボイルの法則のイメージ
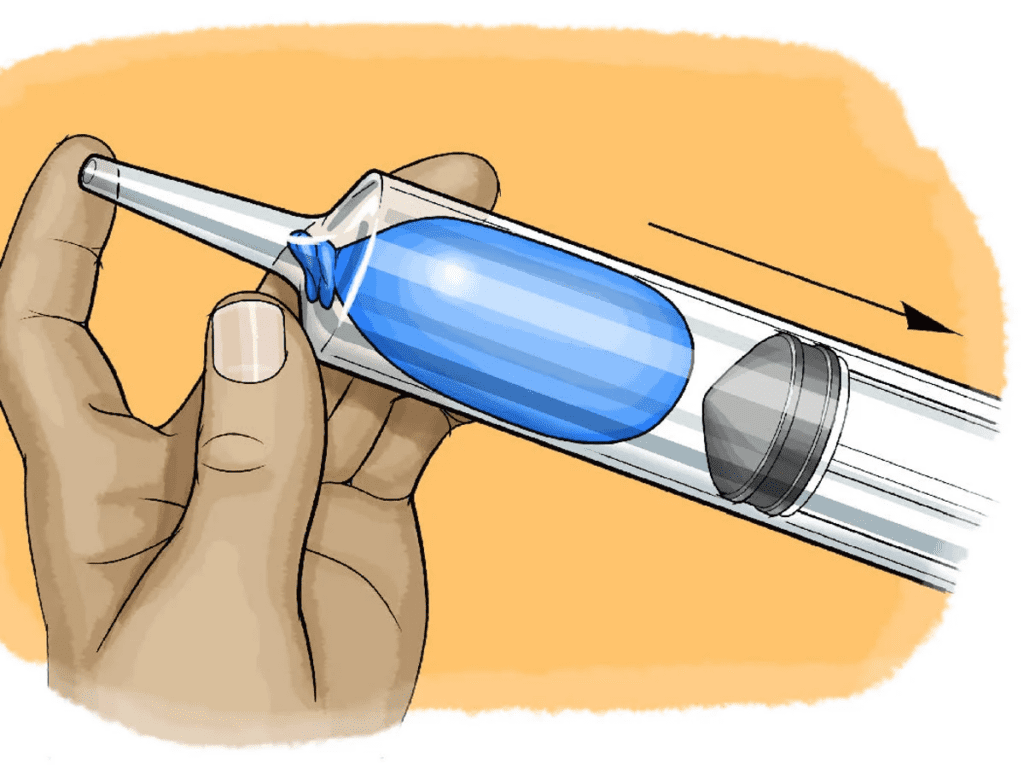
例えば、注射器を想像してみてください。
注射器の先端を指でふさいだままピストンを押すと、内部の空気は圧縮されます。
このとき
- 体積は小さくなる
- 圧力は大きくなる
という変化が起こります。
これはまさにボイルの法則が働いている例です。
シャルルの法則
シャルルの法則とは
シャルルの法則は、フランスの科学者 ジャック・シャルルによって発見された法則です。
この法則は次の関係を示します。
圧力が一定のとき、気体の体積は絶対温度に比例する
式で書くと次のようになります。TV=一定
つまり、
- 温度が2倍 → 体積も2倍
- 温度が3倍 → 体積も3倍
という関係になります。
シャルルの法則のイメージ

わかりやすい例として熱気球があります。
熱気球では、バーナーで空気を温めます。
すると
- 空気の温度が上昇
- 体積が膨張
- 密度が小さくなる
その結果、周囲の空気より軽くなり、熱気球は空へ浮かび上がります。
これもシャルルの法則の応用です。
ボイル・シャルルの法則
二つの法則をまとめたもの
ボイルの法則とシャルルの法則を組み合わせると、次の式になります。TPV=一定
これがボイル・シャルルの法則です。
状態1と状態2を比較すると次の式になります。T1P1V1=T2P2V2
ここで
- P:圧力
- V:体積
- T:絶対温度
を表します。
つまり、圧力・体積・温度の三つの関係を同時に扱える法則なのです。
この法則では、
- 圧力
- 体積
- 温度
の三つが互いに影響し合っています。
例えば
温度が上昇すると
- 体積が増える
- 圧力も変化する
といったように、気体の状態は複雑に変化します。
その変化を数式で整理したものがボイル・シャルルの法則です。
ボイル・シャルルの法則の具体例
① スプレー缶
スプレー缶を火の近くに置いてはいけない理由は、この法則で説明できます。
温度が上昇すると
- 気体の運動が激しくなる
- 圧力が上昇する
結果として容器の耐圧を超えると爆発する可能性があります。
② タイヤの空気圧
自動車のタイヤでも同じことが起こります。
夏場は温度が高くなるため、
- タイヤ内部の空気の温度が上昇
- 圧力が増加
します。
そのためタイヤの空気圧管理が重要になります。
③ 登山とポテトチップス
山に登ると、ポテトチップスの袋が膨らむことがあります。
これは
- 高地では気圧が低い
- 袋の内部の気体が膨張する
ためです。
これもボイルの法則で説明できます。
気体分子運動論との関係
ボイル・シャルルの法則は、気体分子運動論によって理論的に説明できます。
気体は、無数の分子がランダムに運動している状態です。
特徴は次の通りです。
- 分子は高速で運動している
- 分子同士はほとんど相互作用しない
- 容器の壁に衝突して圧力が生まれる
温度が高くなると分子の運動エネルギーが増加し、容器の壁に強く衝突するようになります。
その結果、
- 圧力が増える
- 体積が膨張する
といった現象が起こるのです。
理想気体の状態方程式
ボイル・シャルルの法則は、さらに発展すると次の式になります。PV=nRT
これは理想気体の状態方程式と呼ばれます。
ここで
- :物質量(mol)
- :気体定数(R=8.314J/(mol⋅K)
を表します。
この式は、気体の性質を理解するうえで非常に重要であり、物理学・化学の多くの分野で使われています。
まとめ
ボイル・シャルルの法則は、気体の基本的な振る舞いを説明する重要な法則です。
ポイントを整理すると次のようになります。
ボイルの法則
温度一定
→ 圧力と体積は反比例PV=一定
シャルルの法則
圧力一定
→ 体積は絶対温度に比例V/T=一定
ボイル・シャルルの法則PV/T=一定
この法則は、
- 熱気球
- スプレー缶
- タイヤ
- 気象
- 化学反応
など、私たちの生活や科学技術のさまざまな分野で応用されています。
気体は目に見えませんが、圧力・体積・温度という三つの量で規則的に振る舞うということを理解すると、自然現象をより深く理解できるようになります。
関連記事→熱力学とは何か?エネルギーと自然法則を理解する科学
<補足>ゲイ・リュサック、アモントン、アボガドロの法則について
ややこしくなるので、詳細は省きますがゲイ・リュサックの法則、アモントンの法則、アボガドロの法則を含めてボイル・シャルルの法則及び理想気体の状態方程式と表現することが多いです。



コメント